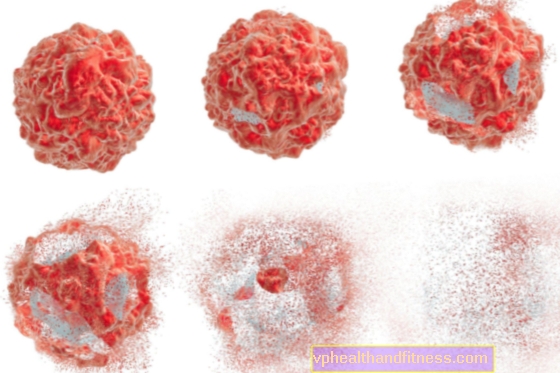
الاستماتة (الاستماتة اليونانية - سقوط الأوراق) هي عملية موت خلوي مبرمج ، وهي ظاهرة طبيعية تمامًا تسمح بإزالة الخلايا غير الطبيعية والتالفة والمستعملة من الجسم. يجدر معرفة ما هو بالضبط ، ما إذا كان موت الخلايا المبرمج ضارًا ، ومتى يحدث وما هي العمليات التي تؤدي إليه.
جدول المحتويات:
- بدء موت الخلايا المبرمج
- مسار موت الخلايا المبرمج
- السيطرة على موت الخلايا المبرمج
- موت الخلايا المبرمج والأمراض
موت الخلايا المبرمج هو عملية فسيولوجية وطبيعية تعمل بشكل مستمر في كل كائن حي سليم ، وهي ضرورية للتشغيل السليم للكائن الحي. بفضل موت الخلايا المبرمج ، يمتلك الجسم القدرة على التحكم في عدد ونوعية الخلايا. تؤدي هذه العملية ، المعروفة باسم موت الخلايا المبرمج ، إلى القضاء على الخلايا التالفة أو المصابة أو غير الضرورية ، مما يضمن التوازن بين تكوين الخلايا الجديدة وتدمير الخلايا القديمة.
الاضطرابات أثناء موت الخلايا المبرمج لها تأثير سلبي للغاية ، فهناك أمراض يصعب الوقاية منها وعلاجها - السرطان وأمراض المناعة الذاتية. ربما ستصبح طرق العلاج الجديدة التي تمكن من عملية موت الخلايا المبرمج في الخلايا السرطانية طريقة فعالة للعلاج.
يتم تحديد العدد الإجمالي للخلايا في الجسم بشكل صارم وثابت ، وأي تغيير طويل الأمد في عددها يمكن أن يكون له تأثير سلبي على صحتنا ، وهذا هو السبب في أن الجسم يسعى للحفاظ على التوازن بين تدمير الخلايا وتكوين خلايا جديدة. يمكن أن تحدث عملية موت الخلايا بعدة طرق ، من أهمها:
- النخر (النخر) - ناتج عن عوامل خارجية: كيميائية ، ميكانيكية ، فيزيائية. إنها عملية مرضية غير طبيعية لا يتحكم فيها الجسم. في مسارها ، يتم تدمير مجموعات كاملة من الخلايا ، ونتيجة هذا الضرر هي تطور العملية الالتهابية.
- يختلف موت الخلايا المبرمج (موت الخلية المبرمج) اختلافًا كبيرًا ، فالعملية طبيعية تمامًا وفسيولوجية وخلية واحدة وضرورية في كائن حي يعمل بشكل طبيعي.
- الالتهام الذاتي - ينطوي على الخلية التي تهضم نفسها عن طريق الإنزيمات الخاصة بها.
على الرغم من تأثيره السلبي ، إلا أن موت الخلايا المبرمج هو ظاهرة طبيعية ومنتظمة ، فهو يهدف إلى إفادة الكائن الحي بأكمله ، مما يسمح باستبدال الخلايا غير الفعالة والمتهالكة بخلايا جديدة. الخلايا التي تمت إزالتها هي بشكل أساسي تلك التي يمكن أن تصبح خطرة على المضيف ، مثل السرطانية أو الورمية
وهكذا ، يساعد موت الخلايا المبرمج في الحفاظ على التوازن ، أي توازن الكائن الحي. إن عملية موت الخلايا المبرمج هي ظاهرة معقدة للغاية ، تنطوي على عشرات الإنزيمات والبروتينات. وقت حدوثها ليس عرضيًا أيضًا ، يتم تحديده من خلال العديد من مسارات الإشارات التي يتم تنشيطها نتيجة لتلف الخلية: عضياتها أو موادها الجينية.
اقرأ أيضًا: Martwica - ما هو؟ أنواع النخر
بدء موت الخلايا المبرمج
يرتبط تنشيط موت الخلايا المبرمج بتنشيط أو تثبيط عمل بعض البروتينات (المؤيدة والمضادة للاستماتة) الموجودة باستمرار في الخلية. تعتمد الطريقة التي تحدث بها العملية على النوع والمحفزات التي تؤدي إلى موت الخلايا المبرمج. البداية هي المرحلة الأولية الأولى ، والتي يتم خلالها تنشيط مسارات الإشارات المؤدية إلى تطوير عملية الموت المبرمج.
أهمها ما يسمى بالمسار الداخلي ، حيث تلعب الميتوكوندريا دورًا مهيمنًا ، والمسار الخارجي ، ومحفزاته هي إشارات من خارج الخلية:
- نقص عوامل النمو والهرمونات
- زيادة في تركيز بعض السيتوكينات (الجزيئات التي تنتجها الخلايا الليمفاوية)
- التفاعلات مع الخلايا المجاورة
- العوامل الفيزيائية
- نقص المغذيات.
في حالة المسار الخارجي ، تعمل المنبهات البيئية على المستقبلات الموجودة في غشاء الخلية (ما يسمى بمستقبلات الموت) ، والتي تؤدي إلى سلسلة من الإشارات داخل الخلايا تؤدي إلى موت الخلايا المبرمج.
في حالة المسار الجوهري ، تلعب الميتوكوندريا دورًا رئيسيًا. بعد تلفها بفعل عوامل مختلفة ، يتم التعبير عن البروتينات المؤيدة للاستماتة في هذه العضيات ، والتي بدورها تلحق الضرر بوظيفة الميتوكوندريا ، مما يمنع إنتاج الطاقة.
بالإضافة إلى ذلك ، يتسبب هذا الضرر في إطلاق بروتين من الميتوكوندريا - السيتوكروم ، مما يساهم في زيادة تركيز أيونات الكالسيوم في الخلية. زيادة كمية هذا الأيون هو سبب لموت الخلايا المبرمج.
مسار موت الخلايا المبرمج
يمكن التعرف على انتقال الخلية إلى موت الخلايا المبرمج من خلال فصلها عن الخلايا الأخرى ، وهي الخطوة الأولى في هذه العملية. ينتج عن تحولات الكهارل وجفاف الخلية والتغيرات في شكلها. ثم يتم تجزئة نواة الخلية وتشكيل ما يسمى بالأجسام الأبوطورية ، وهي عبارة عن بقايا خلوية تمتصها الخلايا المجاورة أو "تأكلها" البلاعم. يؤدي مسار الاستماتة هذا إلى إزالة الخلية "بصمت" ، ولا يتسبب في حدوث تفاعل عام - التهاب.
كما ذكرنا ، تشارك العديد من الإنزيمات في هذه العملية: الكاسبيسات التي تهضم البروتينات الموجودة في النواة والسيتوبلازم ، وإنزيمات الجلوتامينازات المتحولة والإنزيمات المحللة للنواة المسؤولة عن قطع الحمض النووي. يمكن تقسيم مسار عملية التدمير بأكملها (تنفيذ الاستماتة) إلى عدة مراحل:
1. مرحلة قرار التحكم - وهي عبارة عن نقل المعلومات إلى نواة الخلية حول تنشيط آليات الإصلاح أو التخلي عنها وبدء عملية تفكك الخلية. تشارك بروتينات Caspases و BID و BAX في هذه العملية ، وتطلق الخلايا اللمفاوية التائية جرانيزيمات داخل الخلايا ، والتي ، من بين أمور أخرى ، تطلق أيونات الكالسيوم التي تحفز موت الخلايا المبرمج.
2. المرحلة التنفيذية - في هذه المرحلة ، تطور الكاسبيسات وظيفتها الكاملة - تدمر البروتينات الخلوية - الهيكلية والإنزيمية:
- بوليميراز DNA و DNA كيناز ، يمنعان ترميم الأحماض النووية
- الصفائح ، إتلاف الغشاء النووي.
في هذه المرحلة ، يحدث جفاف الخلية ، وتغييرات أخرى في الشكل والحجم ، وتفتيت الحمض النووي (بواسطة نوكلياز داخلي) ، ثم تفتيت الخلية وتشكيل أجسام موت الخلايا المبرمج. هذه الكاسبيسات عبارة عن إنزيمات داخل الخلايا تقطع البروتينات في أماكن محددة - تسلسل معين من الأحماض الأمينية. يتم تنشيطها بطريقة تشبه الانهيار الجليدي - ينشط الكاسبيز المنشط الخطوة التالية.
ومن المثير للاهتمام ، أنه على الرغم من انهيار العديد من البروتينات الخلوية ، تظل العضيات الخلوية غير تالفة وتتغلغل بشكل كامل في أجسام موت الخلايا المبرمج.
3. تعتمد مرحلة التنظيف على البلعمة ، أي امتصاص حطام الخلية ، في أغلب الأحيان بواسطة الخلايا الوهمية - البلاعم.
السيطرة على موت الخلايا المبرمج
موت الخلايا المبرمج هو عملية منظمة بشكل صارم - سواء بدايته أو مساره. عنصر التحكم هو في المقام الأول عائلة البروتينات Bcl-2 ، وهي تشمل البروتينات المضادة للاستماتة - فهي تتعارض مع تطور موت الخلايا المبرمج (على سبيل المثال Bcl-2 و Bcl-XL و Bcl-w) و pro-apoptotic - مما يعزز حدوثه عن طريق إتلاف غشاء الميتوكوندريا (Bid ، Bak ، سيئة).
يعتمد تعبير أو نشاط هذه البروتينات على الظروف التي توجد فيها الخلية ، بالإضافة إلى حالتها - إذا كان الضرر كبيرًا أو الظروف الخارجية غير مواتية ، يتم تنشيط البروتينات المؤيدة للاستماتة.
في ظل الظروف العادية ، تهيمن البروتينات المضادة للاستماتة وتثبط عملية موت الخلايا المبرمج. علاوة على ذلك ، فقد ثبت أن موت الخلايا المبرمج يتحكم فيه أيضًا الجينات ، أحدها هو الجين p53 ، الذي ينتمي إلى العوامل المؤيدة للاستماتة. يُطلق منتجها ، البروتين p53 ، عملية موت الخلايا الانتحارية إذا كان الضرر الذي يلحق بالمادة الجينية شديدًا بحيث يتعذر إصلاح الحمض النووي.
وبالتالي ، يُشار إلى هذا البروتين أحيانًا باسم "حارس الجينوم" لأنه يحدد ما إذا كانت الخلية ستوقف انقسام الخلية لإصلاح الضرر الذي حدث ، أو ما إذا كانت ستتوقف عن موت الخلايا المبرمج.
موت الخلايا المبرمج والأمراض
لقد ثبت أن عدم التوازن بين تكوين الخلايا الجديدة والقضاء على الخلايا القديمة هو سبب العديد من الأمراض ، لذلك فإن التحكم الخلوي في موت الخلايا المبرمج مهم للغاية ، وقد يكون لاضطرابها عواقب وخيمة للغاية.
إذا كانت الخلايا مقاومة للموت عن طريق موت الخلايا المبرمج ، فقد يتطور السرطان أو أحد أمراض المناعة الذاتية (مثل التهاب المفاصل الروماتويدي). في كلتا الحالتين ، لا تخضع الخلايا المريضة لعملية موت الخلايا المبرمج ، فهي "مقاومة" لها بسبب الطفرات الجينية أو النشاط غير الطبيعي للبروتينات المؤيدة والمضادة للاستماتة. من ناحية أخرى ، يمكن أن يؤدي الامتثال المفرط والتخلص من العديد من الخلايا إلى أمراض تنكسية وتلف الأعضاء.
تعمل أحدث عقاقير الأورام التي تم اختبارها حاليًا في مرحلة موت الخلايا المبرمج - وتتمثل آلية العمل في تعزيز وجود البروتينات المؤيدة للاستماتة - مما يعزز حدوث موت الخلايا المبرمج في الخلايا السرطانية. يعمل العلاج الإشعاعي والعلاج الكيميائي "القياسي" بطريقة مماثلة للحث على موت الخلايا المبرمج. كلا هذين العلاجين يسببان إجهادًا خلويًا يقتل الخلايا السرطانية. لسوء الحظ ، لا يكون هذا العلاج فعالًا دائمًا ، لأن نشاط العوامل المثبطة لموت الخلايا المبرمج لا يزداد بشكل متكرر في الخلايا السرطانية ، مما لا يعيق محاربتها فحسب ، بل يؤدي أيضًا إلى النمو والتكاثر غير المنضبطين.
اقرأ أيضًا: تطور السرطان ، أو كيف ينشأ السرطان
مقال موصى به:
تطور الورم - كيف يتكون السرطان عن المؤلف


---czym-jest-realizacja-e-recepty.jpg)
---badanie-ktre-tropi-paciorkowce-i-chorob-reumatyczn.jpg)












-pomocne-w-agodzeniu-menopauzy.jpg)