الأربعاء 17 أبريل ، 2013. - انتهى الباحثون في جامعة سالامانكا من إجراء تحقيق يوضح فعالية العلاج المبني على إعطاء هرمون النمو مع إعادة التأهيل لدى الفئران البالغة التي تعاني من إصابات في الدماغ. توضح النتائج ، التي نشرت في مجلة "أبحاث الدماغ السلوكية" ، كيف تستعيد الحيوانات وظائفها الحركية عندما يبدأ العلاج فور حدوث الإصابة.
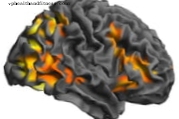
هذا الاكتشاف هو جزء من التحقيق الذي بدأ منذ سنوات ويركز على فوائد عمليات زرع العصب في نماذج الفئران مع آفة من القشرة الحركية ، وهي جزء من القشرة الدماغية التي تتحكم في الحركات التطوعية وتنفذها.
في النموذج الجديد ، يتم تعليم الحيوانات أولاً سلوكًا جيدًا في المهارات الحركية ، والذي يتكون من سحب الساق من خلال إحدى الثقوب الموجودة في مربع الاختبار للوصول إلى الطعام الموجود في وحدة التغذية.
بمجرد معرفة هذا السلوك ، يتم إجراء آفة شفط في القشرة الحركية المقابلة على أيديهم المفضلة ، بحيث إذا كان فأرًا في اليد اليمنى ، يصاب نصف الكرة الأيسر ، وإذا أصيب في نصف الكرة الأيسر الحق ، لأن كل نصف الكرة المخية تسيطر على الطرف الآخر. بعد التحقق من أن الآفة فعالة ، ننتقل إلى إجراء عمليات زرع عصبية.
بدأ المؤلفون في إجراء عمليات الزرع هذه من أنسجة جنينية من نفس منطقة المخ ، والتحقق من وجود انتعاش للوظائف الحركية ، ودراسة الآليات المشاركة في الشفاء باستخدام أنواع مختلفة من الأنسجة المانحة غير القشرية ، مثل أنسجة أو نواة مخططة.
عند التفكير في نقل هذه التحقيقات إلى الإنسان ، ومع الأخذ في الاعتبار المشكلات الأخلاقية والقانونية المرتبطة باستخدام الأنسجة الجنينية ، فكر العلماء في معالجة الاستراتيجيات الأخرى. أحدها كان استخدام الخلايا النجمية ، وهي نوع من الخلايا الدبقية ، مغلفة في كرات ألجينات ، وهي بوليمر متوافق حيويا.
ومع ذلك ، حدث تغيير في البحث عن استراتيجيات جديدة
من خلال التعاون مع Jesús Devesa ، باحث في جامعة سانتياغو دي كومبوستيلا وهو رائد في العلاجات السريرية مع هرمون النمو. تقول مارغريتا هيريديا: "لقد اتصلنا به لتطبيق أسلوبه على نموذجنا التجريبي".
تتكون هذه المرحلة الجديدة من تطبيق هرمون النمو إلى جانب إعادة التأهيل للفئران البالغة مشروطة بإجراء اختبار المهارة الحركية الدقيقة ، والتي أصيبت لاحقًا بالشفط في القشرة الحركية والتي أثبتت فعالية الآفة فيها.
لإجراء التجارب ، تم تقسيم الفئران إلى عدة مجموعات. تم تطبيق أحدهم على هرمون النمو مباشرة بعد الإصابة وآخر في ستة أيام. والنتيجة ، المؤيدة من قبل مجموعات أخرى من الحيوانات التي تعمل بمثابة عنصر تحكم للتجربة ، هي أن الفئران من المجموعة الأولى قد وصلت إلى الشفاء الوظيفي للعجز الحركي وأن الفئران الثانية لم تصل.
تتم إعادة التأهيل ، التي تنطوي على إجبار استخدام اليد المتأثرة بالإصابة ، على فترتين ، بين 5 و 14 يومًا من الإصابة و 30 يومًا بعد العلاج بهرمون النمو ، على الرغم من أن الباحثين يفكرون الآن في تقديم الأطر الزمنية الأخرى.
من ناحية أخرى ، شملت الأبحاث أيضًا دراسات مناعية كيميائية لتحديد المواد المشاركة في هذه العمليات. أحدها هو البروتين الحمضي الليفي (GFAP) ، والذي يزداد بعد الإصابة بسبب تفاعل الخلايا النجمية الذي يحدث في منطقة الآفة.
تعاملت الدراسة أيضًا مع nestin ، وهو بروتين يتم التعبير عنه أثناء التطور في الخلايا السلف العصبية وفي الدماغ البالغ يوجد أساسًا في الأماكن التي توجد فيها الخلايا الجذعية ، مثل البطينين الجانبيين أو الحصين. وبهذا المعنى ، تحققوا من إعادة التعبير عن اللقمة بعد الإصابة.
بعد هذا المنشور ، يقترح باحثون من جامعة سالامانكا تجارب جديدة يبدأ فيها التأهيل من اليوم الأول من علاج هرمون النمو ، بالإضافة إلى تحليل دور مستقبلات هرمون النمو.
المصدر:
علامات:
الأدوية قطع والطفل أخبار
هذا الاكتشاف هو جزء من التحقيق الذي بدأ منذ سنوات ويركز على فوائد عمليات زرع العصب في نماذج الفئران مع آفة من القشرة الحركية ، وهي جزء من القشرة الدماغية التي تتحكم في الحركات التطوعية وتنفذها.
في النموذج الجديد ، يتم تعليم الحيوانات أولاً سلوكًا جيدًا في المهارات الحركية ، والذي يتكون من سحب الساق من خلال إحدى الثقوب الموجودة في مربع الاختبار للوصول إلى الطعام الموجود في وحدة التغذية.
بمجرد معرفة هذا السلوك ، يتم إجراء آفة شفط في القشرة الحركية المقابلة على أيديهم المفضلة ، بحيث إذا كان فأرًا في اليد اليمنى ، يصاب نصف الكرة الأيسر ، وإذا أصيب في نصف الكرة الأيسر الحق ، لأن كل نصف الكرة المخية تسيطر على الطرف الآخر. بعد التحقق من أن الآفة فعالة ، ننتقل إلى إجراء عمليات زرع عصبية.
بدأ المؤلفون في إجراء عمليات الزرع هذه من أنسجة جنينية من نفس منطقة المخ ، والتحقق من وجود انتعاش للوظائف الحركية ، ودراسة الآليات المشاركة في الشفاء باستخدام أنواع مختلفة من الأنسجة المانحة غير القشرية ، مثل أنسجة أو نواة مخططة.
عند التفكير في نقل هذه التحقيقات إلى الإنسان ، ومع الأخذ في الاعتبار المشكلات الأخلاقية والقانونية المرتبطة باستخدام الأنسجة الجنينية ، فكر العلماء في معالجة الاستراتيجيات الأخرى. أحدها كان استخدام الخلايا النجمية ، وهي نوع من الخلايا الدبقية ، مغلفة في كرات ألجينات ، وهي بوليمر متوافق حيويا.
ومع ذلك ، حدث تغيير في البحث عن استراتيجيات جديدة
من خلال التعاون مع Jesús Devesa ، باحث في جامعة سانتياغو دي كومبوستيلا وهو رائد في العلاجات السريرية مع هرمون النمو. تقول مارغريتا هيريديا: "لقد اتصلنا به لتطبيق أسلوبه على نموذجنا التجريبي".
تتكون هذه المرحلة الجديدة من تطبيق هرمون النمو إلى جانب إعادة التأهيل للفئران البالغة مشروطة بإجراء اختبار المهارة الحركية الدقيقة ، والتي أصيبت لاحقًا بالشفط في القشرة الحركية والتي أثبتت فعالية الآفة فيها.
لإجراء التجارب ، تم تقسيم الفئران إلى عدة مجموعات. تم تطبيق أحدهم على هرمون النمو مباشرة بعد الإصابة وآخر في ستة أيام. والنتيجة ، المؤيدة من قبل مجموعات أخرى من الحيوانات التي تعمل بمثابة عنصر تحكم للتجربة ، هي أن الفئران من المجموعة الأولى قد وصلت إلى الشفاء الوظيفي للعجز الحركي وأن الفئران الثانية لم تصل.
تتم إعادة التأهيل ، التي تنطوي على إجبار استخدام اليد المتأثرة بالإصابة ، على فترتين ، بين 5 و 14 يومًا من الإصابة و 30 يومًا بعد العلاج بهرمون النمو ، على الرغم من أن الباحثين يفكرون الآن في تقديم الأطر الزمنية الأخرى.
من ناحية أخرى ، شملت الأبحاث أيضًا دراسات مناعية كيميائية لتحديد المواد المشاركة في هذه العمليات. أحدها هو البروتين الحمضي الليفي (GFAP) ، والذي يزداد بعد الإصابة بسبب تفاعل الخلايا النجمية الذي يحدث في منطقة الآفة.
تعاملت الدراسة أيضًا مع nestin ، وهو بروتين يتم التعبير عنه أثناء التطور في الخلايا السلف العصبية وفي الدماغ البالغ يوجد أساسًا في الأماكن التي توجد فيها الخلايا الجذعية ، مثل البطينين الجانبيين أو الحصين. وبهذا المعنى ، تحققوا من إعادة التعبير عن اللقمة بعد الإصابة.
بعد هذا المنشور ، يقترح باحثون من جامعة سالامانكا تجارب جديدة يبدأ فيها التأهيل من اليوم الأول من علاج هرمون النمو ، بالإضافة إلى تحليل دور مستقبلات هرمون النمو.
المصدر: